来源: 时间:2025-10-09 16:33:27 点击量:
近日,山东第一医科大学附属皮肤病医院张福仁/刘红课题组在国际权威期刊《Signal Transduction and Targeted Therapy》发表题为“TSC22 domain family member 3 links natural killer cells to CD8+ T cell-mediated drug hypersensitivity”的研究论著,系统揭示了自然杀伤(NK)细胞在重症药物不良反应(SCAR)发病机制中的关键作用。这项研究首次阐明了NK细胞通过TSC22D3基因调控CD8+ T细胞活化的分子机制,为理解这类致命性药物反应提供了全新的免疫学视角。
SCAR是由T细胞介导的、可致死的重症皮肤病,而这类疾病与人体内的HLA基因密切相关。研究发现,特定的HLA基因型(如HLA-B*13:01与氨苯砜过敏、HLA-B*15:02与卡马西平过敏等)是SCAR的关键风险因素。虽然基因检测能有效排除高风险人群(阴性预测值近100%),但携带这些基因的人并非都会发病(阳性预测值仅3-50%)。这意味着,即使检测出高风险基因,多数人仍可安全用药。因为SCARs的发生不仅依赖HLA基因,还涉及免疫系统的其他调控因素。
研究团队以氨苯砜超敏综合征(DHS)为模型,通过单细胞转录组测序和体内外功能验证实验,发现DHS患者外周血中NK细胞不仅数量显著减少,更重要的是表现出明显的功能异质性。其中效应型NK细胞亚群(CD56high XCL1/2high)呈现过度活化状态,能够分泌大量颗粒酶B(GZMB)和颗粒溶素(GNLY)等细胞毒性分子,直接促进CD8+ T细胞的炎症反应。与此同时,具有免疫调节功能的NK细胞亚群(CD56low XCL1/2low)数量明显减少,导致其对T细胞活化的抑制作用减弱。这种NK细胞亚群平衡的破坏与TSC22D3基因的低表达密切相关。进一步的机制研究表明,TSC22D3的表达下调会显著增强NK细胞的细胞毒性功能,进而推动CD8+ T细胞介导的过度免疫应答,最终导致SCAR的发生(图1)。
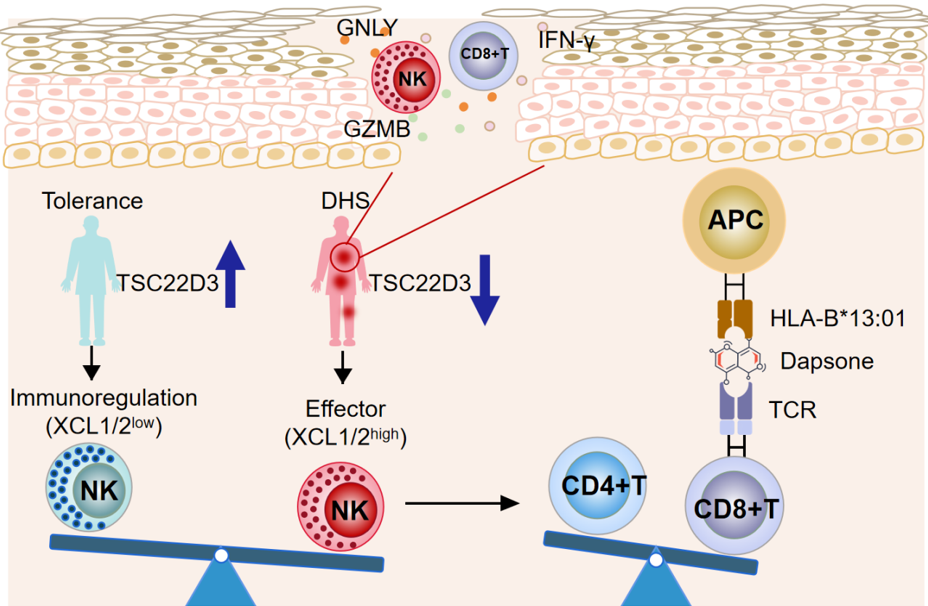
图1. NK细胞介导SCAR发病示意图
从临床转化角度来看,这项研究提出了SCAR防控的新策略。在预防层面,除了现有的HLA基因筛查外,增加NK细胞功能评估(如效应/调节亚群比例分析或TSC22D3表达检测)可以显著提高阳性预测值。在治疗方面,靶向调控NK细胞功能可能成为新的干预方向,包括使用TSC22D3激动剂来抑制效应型NK细胞的过度活化或者恢复调节型NK细胞的功能。更长远来看,开发同时靶向NK细胞和CD8+ T细胞的联合治疗方案可能提供更好的临床疗效。
这项研究是团队十年系统研究的延续和突破。早在2013年,团队就率先发现HLA-B*13:01是DHS的关键风险基因(N Engl J Med 2013),并成功将其转化为临床应用,通过全国范围内的用药前筛查使DHS发病率从3.1%降至0(JAMA Dermatol 2019)。随后的系列研究逐步揭示了DHS的免疫学机制,包括发现氨苯砜及其代谢产物(亚硝基氨苯砜)分别通过P-I理论和半抗原理论激活T细胞(Allergy 2019;J Invest Dermatol 2021),阐明TAP基因甲基化通过TNF-α-VISTA轴调控T细胞活化阈值(J Invest Dermatol 2023;Allergy 2024)等重要发现。最新关于NK细胞的研究突破不仅完善了DHS发病的机制图景(图2),更重要的是开辟了新的研究和干预方向。
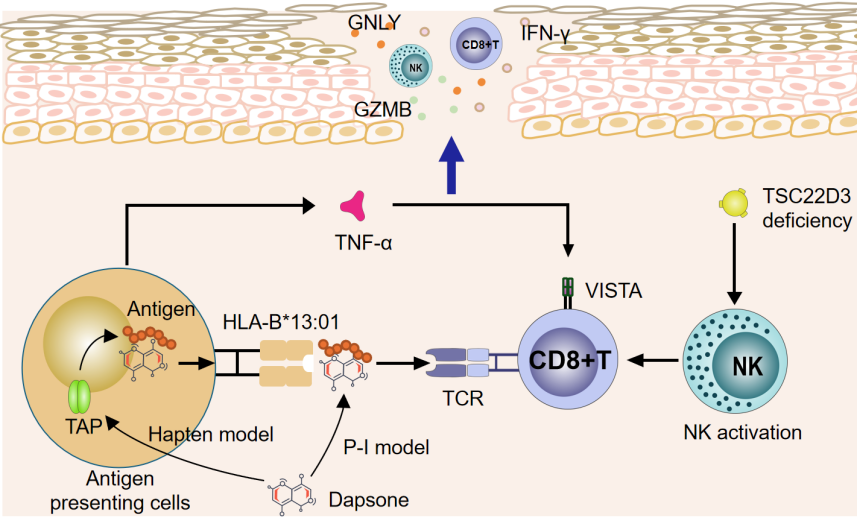
图2. DHS发病示意图
本文第一作者单位为山东第一医科大学附属皮肤病医院,第一作者为孙乐乐副研究员,通讯作者为山东第一医科大学附属皮肤病医院的刘红教授/张福仁教授。本研究得到了山东省重点研发计划、国家自然科学基金、山东省泰山学者项目及山东第一医科大学临床-基础联合创新团队项目的资助。
原文链接:
https://pmc.ncbi.nlm.nih.gov/articles/PMC12182574/pdf/41392_2025_Article_2300.pdf
通讯员:林颖杰